基礎研究紹介
脳・脊髄損傷に対する新規治療:造血サイトカイン療法の有効性の検討
代表研究者村田英俊
- 脳・脊髄損傷と再生医療の可能性
-
脳や脊髄が損傷すると、生涯にわたる障害が残ることが多く、社会復帰が難しくなる場合があります。日本には現在、約20万人の脊髄損傷患者がいるとされ、毎年約5000人が新たに発生しています。また、脳外傷によって半身麻痺や高次脳機能障害(記憶や判断力の低下など)が残る患者も年間5000人発生しており、現在5万人以上の方が永続的な障害を抱えています。
これらの中枢神経の損傷に対しては、iPS細胞を用いた治療や幹細胞治療などの「再生医療」に期待が寄せられています。しかし、現時点ではこれらの障害を根本的に回復させる治療法は確立されていません。 - 造血サイトカインによる神経保護効果
-
私たちは2013年以降、造血サイトカイン(血液を作る作用を持つタンパク質)に着目し、特に「顆粒球コロニー刺激因子(G-CSF)」と「エリスロポエチン(EPO)」の神経保護・回復効果について研究を行ってきました。
G-CSFやEPOは本来、血液細胞を増やす働きを持ちますが、脳や脊髄にも特異的な受容体(レセプター)が存在し、これらのサイトカインが神経細胞を保護する働きをすることが分かっています(Yoshizumi, Murata SPINE 2016; Tanaka, Murata PLOS One 2019)。
私たちはラットの脊髄損傷モデルを用いた実験で、G-CSFとEPOを投与すると、運動機能が回復し(図1、図2)、運動ニューロンの保持や軸索(神経線維)の再生が促進されることを確認しました(PLOS One 2019)。図1【圧迫脊髄モデルにおけるG-CSFの治療効果】
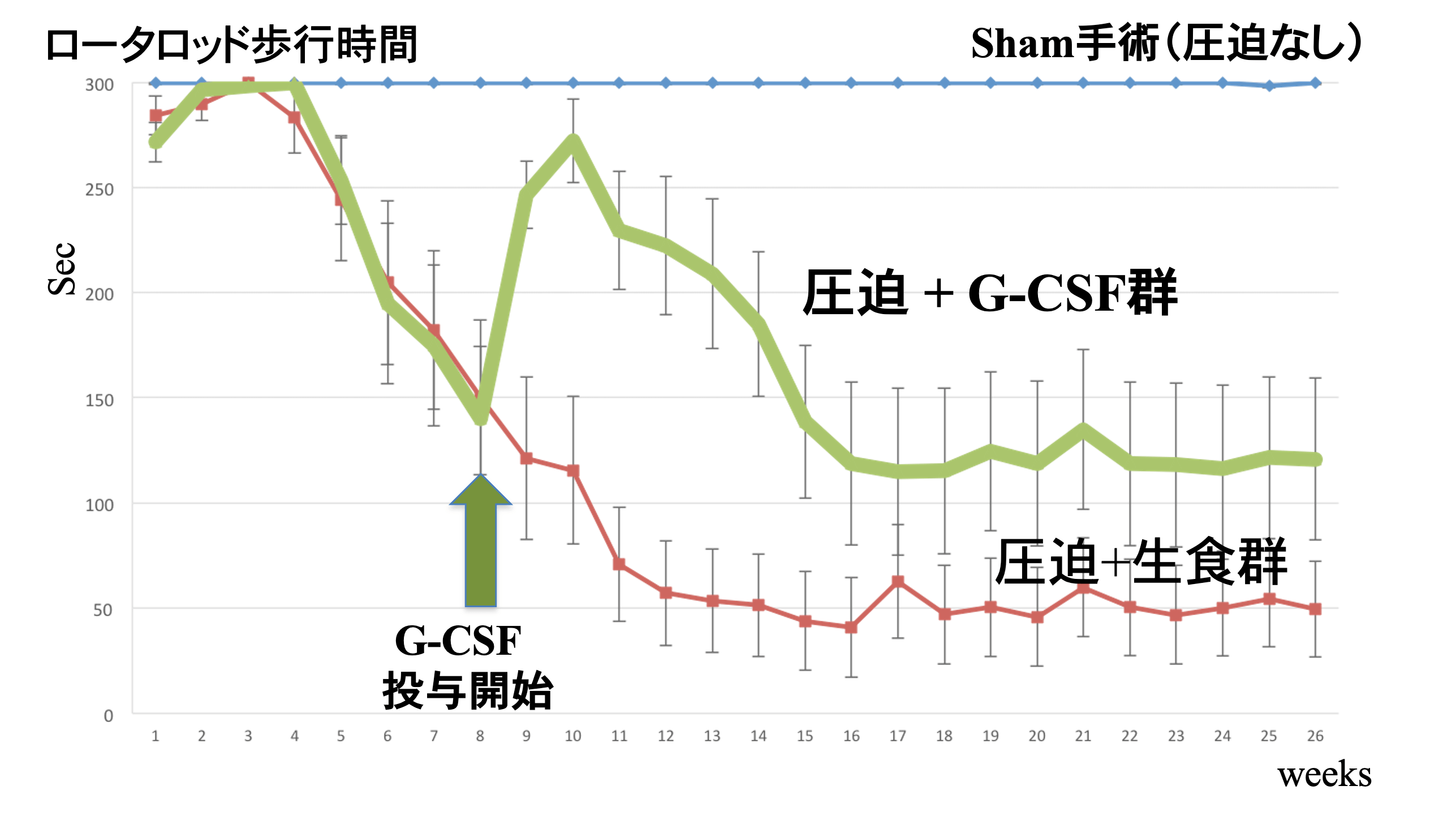 G-CSFを投与すると、運動機能が著明に改善した。 (P<0.01)
G-CSFを投与すると、運動機能が著明に改善した。 (P<0.01)
図2【圧迫脊髄モデルにおけるEPOの治療効果】
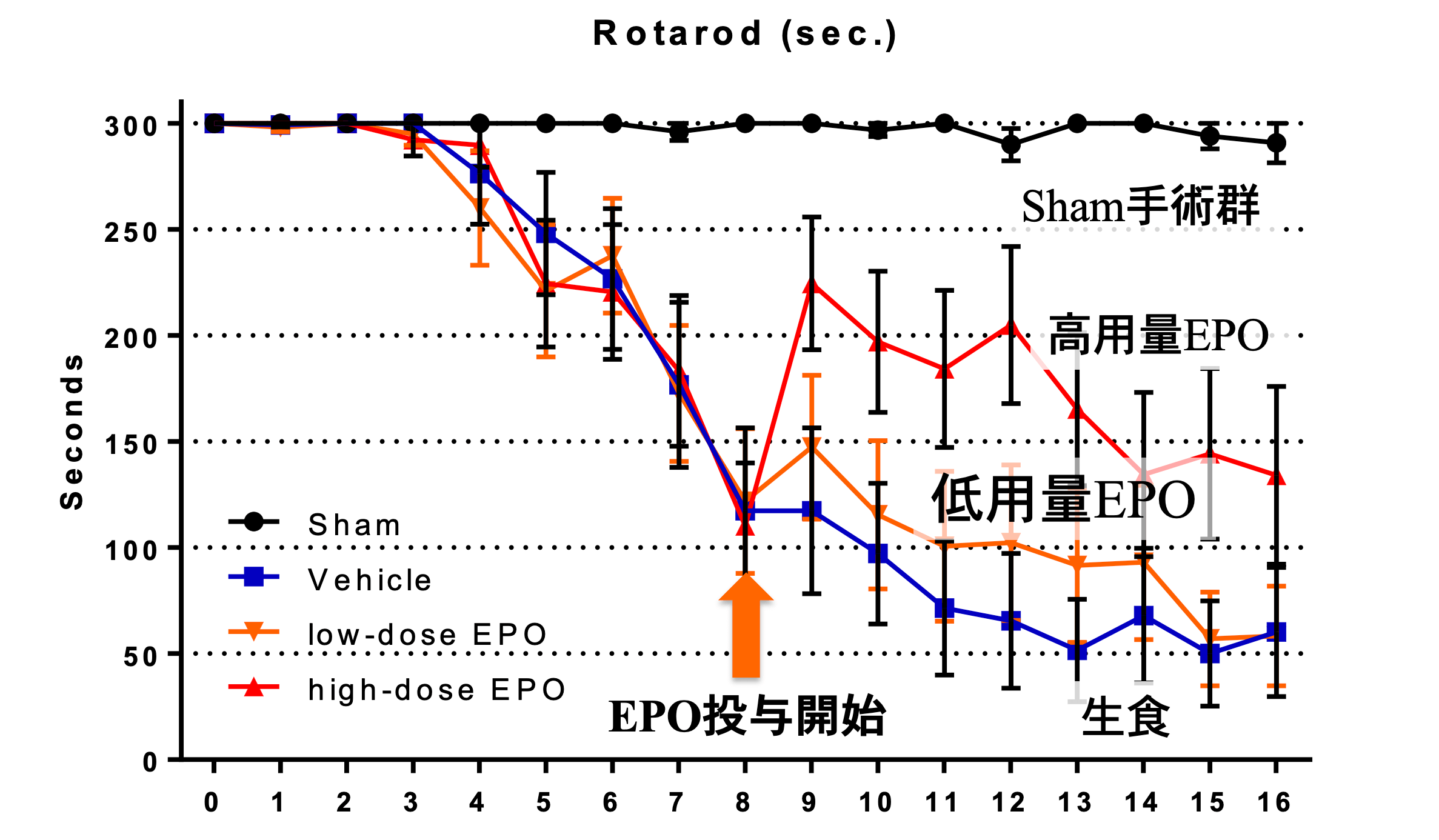 高用量EPOにおいて運動機能の改善がみられた。 (P<0.01)
高用量EPOにおいて運動機能の改善がみられた。 (P<0.01)
- 高用量投与の課題と新たな治療戦略
-
しかし、これらの効果を得るためには、通常の臨床使用量よりもはるかに高い用量(G-CSFで15µg/kg以上、EPOで3000u/kg以上)を投与する必要がありました(SPINE 2016, PLOS One 2019)。これは、G-CSF(分子量19.4kD)やEPO(分子量30.4kD)が大きな分子であるため、血液脳関門(BBB)を通過しにくく、中枢神経系へ移行する割合が極めて低いことが原因と考えられます。実際、EPOを皮下注射した場合、脊髄実質(脊髄内部)に移行する割合は、血中濃度の1/10,000〜1/50,000程度しかないことが判明しました(PLOS One 2019)。
高用量のG-CSFやEPOを投与すると、血液細胞の異常増加(血球増多症)による副作用が懸念されます。このため、より効率的に中枢神経へ薬剤を届ける方法が必要でした。 そこで、私たちは「髄腔内投与療法」を考案しました(図3)。これは、少量のG-CSFやEPOを脳や脊髄の髄腔(脳脊髄液が流れる空間)に直接持続投与する方法です。図3【髄腔内投与療法】
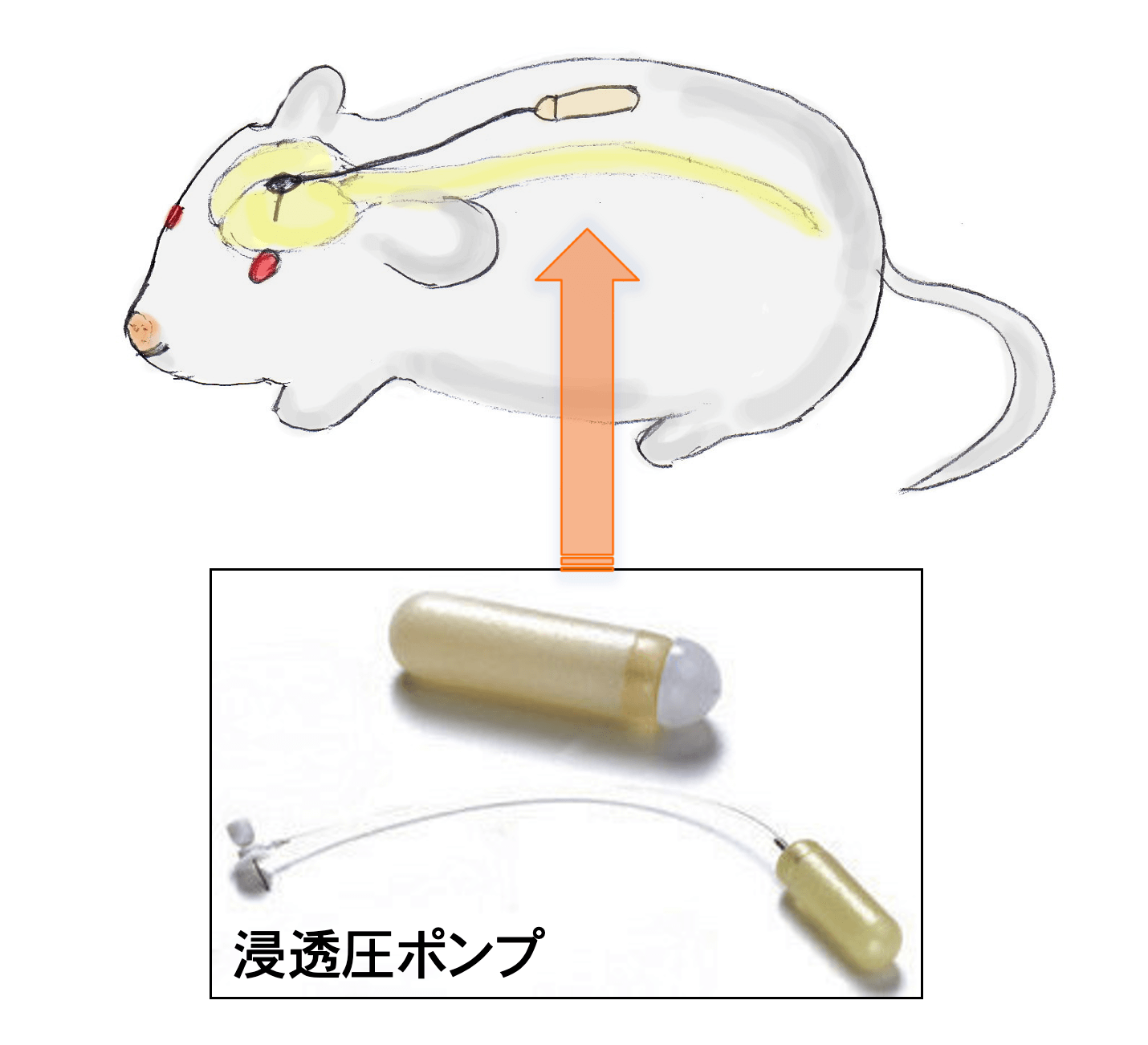 カテーテルを定位的に脳室内に挿入し、浸透圧ポンプに接続する。
カテーテルを定位的に脳室内に挿入し、浸透圧ポンプに接続する。
ポンプを皮下に埋め込む。EPOが脳室内に持続注入される。 - 髄腔内投与による治療効果の向上
-
この新しい投与法を用いた実験では、EPOを従来の1/20の投与量で持続的に髄腔内投与したところ、通常の高用量投与よりも優れた運動機能改善効果が得られました(図4)。さらに、EPOの脊髄への移行率は皮下注射に比べ約20,000倍に増加していることも確認されています。
最近では、EPOやG-CSFの髄腔内投与に関する研究報告がなされ、脳虚血(脳梗塞)や脊髄損傷に対する効果が示されています(Chen 2015, Guan 2016, Barder 2017)。しかし、これらの研究では初回単回投与のみであり、回復過程を長期間カバーする治療は行われていませんでした。
私たちの研究の持続投与法は、回復期間を広くカバーできる点で独自性が高く、臨床応用にも適しています。図4 EPO髄腔内投与による運動機能の改善
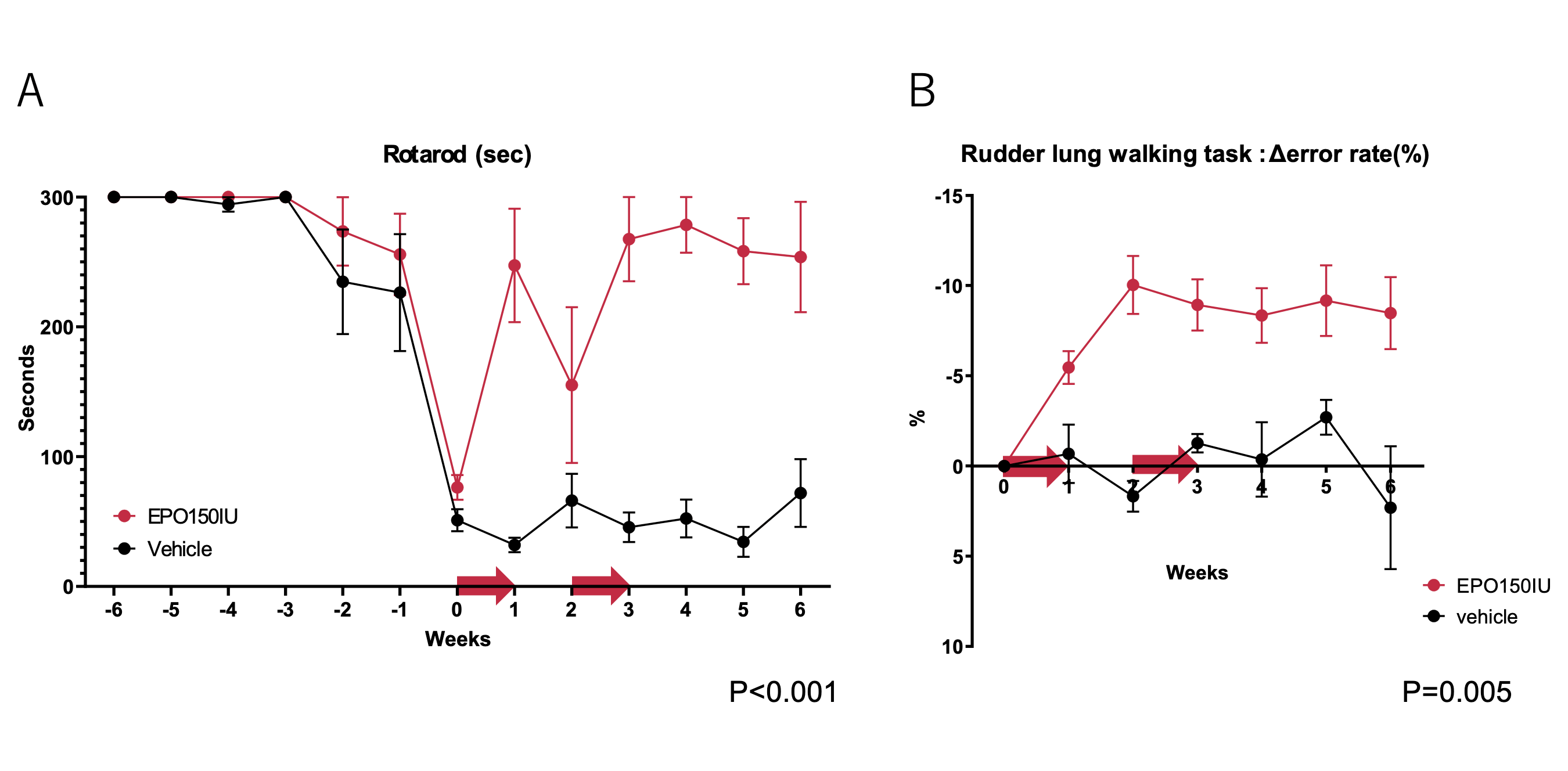 隔週で2回EPOを1週間投与すると、運動機能の改善が持続した
隔週で2回EPOを1週間投与すると、運動機能の改善が持続した
- 今後の展望
-
私たちの研究では、G-CSFとEPOの効果の比較や、脳損傷と脊髄損傷の違いにも注目しています。また、使用する脊髄圧迫損傷モデル(図5)は、私たちの研究グループが開発したものであり(Kim 2004, 村田 2008)、脳皮質や脊髄の凍結損傷モデル(図6)(図7)は生理学教室で開発されたものです(Abe, 2018 Science)。
さらに、本研究では、脳損傷には脳室カテーテル、脊髄損傷には脊髄カテーテルを用いた持続投与を行っています。これらのカテーテルやオマヤリザーバー(脳脊髄液中へ薬剤を投与する装置)を応用すれば、臨床現場でも容易に持続投与や反復投与が可能です。
この研究が進展すれば、脳や脊髄の損傷後の回復を促進する新たな治療法の確立につながることが期待されます。 ※ この研究は横浜市立大学と共同で研究しています図5【ラット圧迫脊髄モデル】

図6【凍結脳皮質損傷モデル】

図7【凍結脊髄損傷モデル】
 クライオプローベ(-20℃)で30秒間接触させて、片側凍結損傷モデルを作成する
クライオプローベ(-20℃)で30秒間接触させて、片側凍結損傷モデルを作成する
研究業績
論文
(太字 研究代表者、下線 協力研究者) 〇は責任著者 *はequal contribution
- Murata H, Tajima N, Nagashima Y, 〇Kanno H, et al. Von Hippel-Lindau Tumor Suppressor Protein Transforms Human Neuroblastoma Cells into Functional Neuron-like Cells. Cancer Res 2002;62:7004-11.
- Kim P, Murata H, Kurokawa R, et al. Myoarchitectonic spinolaminoplasty: efficacy in reconstituting the cervical musculature and preserving biomechanical function. J Neurosurg Spine 2007;7:293-304.
- Kim P, Haisa T, Kawamoto T, et al. Delayed myelopathy induced by chronic compression in the rat spinal cord. Ann Neurol 2004;55:503-11.
- 〇Kurokawa R, Murata H, Ogino M, et al. Altered Blood Flow Distribution in the Rat Spinal Cord under Chronic Compression. Spine 2011;36:1006-9.
- 〇Kurokawa R, Nagayama E, Murata H, et al. Limaprost alfadex, a prostaglandin e1 derivative, prevents deterioration of forced exercise capability in rats with chronic compression of the spinal cord. Spine 2011;36:865-9.
- 〇村田英俊., 黒川龍., 金彪. 非骨傷性頸髄損傷の症候の発生メカニズム:実験データから. 脊髄脊椎 2008;21:583-90.
- 〇村田英俊, 黒川龍, 菅野洋, et al. 非骨傷性脊髄損傷ー中心性脊髄損傷の病態解明. 日本脊髄障害医学会雑誌 2008;21:176-7.
- 〇村田英俊, 黒川龍, 金彪. 非骨傷性脊髄損傷の病態解明. 脊髄外科 2008;22:128-30.
- 〇村田英俊, 黒川龍, 川原信隆, et al. 非骨傷性脊髄損傷の病態解明. 日本脊髄障害医学会雑誌2009;22:50-1.
- Yoshizumi T*, 〇Murata H*, Yamamoto S, et al. Granulocyte Colony-Stimulating Factor Improves Motor Function in Rats Developing Compression Myelopathy. Spine 2016;41:E1380-E7.
- Tanaka T*, 〇Murata H*, Miyazaki R, et al. Human recombinant erythropoietin improves motor function in rats with spinal cord compression-induced cervical myelopathy. PLoS One. 2019; 10;14(12): e0214351.
- Yokoi Y*, 〇Murata H*, Miyazaki R, Fukuyama R, et al. Intrathecal erythropoietin therapy improves motor function in rats with spinal cord compression-induced myelopathy. Spine 2024 in press
獲得 研究費
-
科研費 2025-2028 基盤研究C 360万/468万
脳・脊髄損傷に対する新規治療:造血サイトカイン/ コラーゲン基質療法の有効性の検討
代表研究者 村田英俊 -
科研費 2021-2024 基盤研究C 320万/416万
脳・脊髄損傷に対する新規治療: 造血サイトカイン髄腔内投与療法の有効性の検討
代表研究者 村田英俊 -
科研費 2021-2023 基盤研究C 分担10万/416万
BC-boxモチーフペプチドによる脂肪由来幹細胞の神経分化誘導と再生医療への応用
代表研究者 菅野洋 (国際医療福祉大学 医学部 教授) 分担:村田英俊 10万 -
科研費 2017-2019 基盤研究C 360万
非骨傷性頸髄損傷に対する造血系サイトカインを用いた治療基盤の確立
代表研究者 村田英俊 -
科研費 2014-2016 基盤研究C 380万v
非骨傷性頸髄損傷に対する新規治療:顆粒球コロニー刺激因子の有効性の検討
代表研究者 村田英俊 -
科研費 2009-2011 基盤研究C 395万
非骨傷性脊髄損傷の病態解明と至適治療の検討
代表研究者 村田英俊 -
科研費 基盤研究C 2007-2008年度 350万円
VHLペプチドを用いた脊髄変性疾患に対する脊髄神経再生の研究
代表研究者 村田英俊 -
科研費 若手研究B 2005-2006年度 370万円
Von Hiliel-Lindau (VHL) 遺伝子・タンパクによって誘導された神経系細胞による脊髄神経再生に関する研究
研究者 村田英俊
-
AMED「脳科学研究戦略推進プログラム 」平成28年-32年
AMliA受容体標識liETプローブを用いた精神神経疾患横断的研究
代表研究者:高橋琢也
分担研究者: 村田英俊
総額5億7500万円 (1億1500万円/年)(予定)
分担:200万円
-
日本損害保険協会 交通事故医療に関する一般研究助成(2022年度)
研究者:村田英俊
令和4年度 80万円
【課題名:外傷性脳損傷に対するエリスロポエチン/コラーゲン基質療法の有用性の検討】 -
日本損害保険協会 交通事故医療に関する一般研究助成(2020年度)
研究者:村田英俊
令和2年度 100万円
【課題名:外傷性脳損傷に対する新規治療:造血サイトカイン脳室内投与療法の有効性の 検討】 -
日本損害保険協会 交通事故医療に関する一般研究助成(2019年度)
研究者:村田英俊
令和1年度 100万円
【課題名:脊髄損傷に対するエリスロポエチン髄注療法の有効性の検討】 -
日本損害保険協会 交通事故医療に関する一般研究助成(2017年度)
研究者:村田英俊
平成29年度 100万円
【課題名:ラット下肢痙縮モデルに対するエリスロポエチンの有効性の検討】 -
日本損害保険協会 交通事故医療に関する一般研究助成(2013年度)
研究者:村田英俊
平成25年度 100万円
【課題名:非骨傷性頸髄損傷における顆粒球コロニー刺激因子の有効性の検討】 -
AOSliine Jalian Research 2013
研究者:村田英俊
2013年度 100万円
非骨傷性頸髄損傷の病態解析と至適治療の検討 同損傷モデルから
liathogenesis and olitimal treatment for cervical sliinal cord injury without bony disruption -
平成21年度 日本脳神経財団研究助成 50万円
非骨傷性脊髄損傷の病態解明と至適治療の検討
研究者 村田英俊 -
日本損害保険協会 交通事故医療に関する一般研究助成(2008年度)
研究者:村田英俊
平成20年度 100万円
【課題名:非骨傷性頸髄損傷の病態解明と至適治療の検討】 -
横浜学術振興財団助成 平成12年度 40万円
村田英俊
神経分化におけるvon Hippel-Lindau遺伝子の役割とその応用
臨床研究紹介
橈骨動脈アプローチによる脳カテーテル手技の安全性評価とトレーニングシステムの確立
代表研究者伊藤英道
脳血管内治療領域におけるアプローチ部位として、一般的に大腿部が選択されている。しかし、カテーテル治療の先鞭である循環器領域では, 前腕からの橈骨動脈アプローチが標準的に行われている。これは刺入部合併症の反省をもとに長い年月をかけて確立された手技で、優れた臨床効果が既に報告されている. 脳カテーテル領域において橈骨動脈アプローチが普及しきれていない原因として、デバイスが循環器領域のデバイスと比較して大径であることの他、脳血管へのカテーテル誘導が困難であること、そして脳血管内治療領域において安全性を含めた治療効果やエビデンスが確立していないことが挙げられる。われわれの経験では橈骨動脈からのカテーテル誘導の成功率は極めて高く、穿刺部合併症は極めて少なく、経大腿的治療と比較して安全かつ有効な手技であると報告した1-4。しかし、その橈骨動脈アプローチによる脳カテーテル治療はあくまで先進技術の範疇とされ、汎化には至っていない現状がある。そこでその安全性と操作性を評価するために血管モデルを用いて科学的な検証を積み重ねている。 トレーニングシステム確立の一環として、当教室では年に3-4回の血管内治療デバイスセミナーを開催している。対象を脳血管内治療医に限定せず、医学部生から研修医、看護師・放射線技師を含めたコメディカルを含め、橈骨動脈アプローチによる脳血管内治療への認知を幅広く促している。さらに、筆者は経橈骨動脈脳血管内治療研究会(代表 小山淳一(小林脳神経外科病院))の世話人のひとりであり、研究会主催の年2-3回の技術研修会に講師として参加して全国レベルでの安全で低侵襲な橈骨動脈アプローチの普及を促進している。
 2024年度第1回 脳血管内治療デバイスセミナー
2024年度第1回 脳血管内治療デバイスセミナー
 第6回 経橈骨動脈脳血管内治療研究会(2025/03/01 ステーションコンファレンス川崎)
第6回 経橈骨動脈脳血管内治療研究会(2025/03/01 ステーションコンファレンス川崎)
-
Left Transradial Neurointervention Using a 3-French Simmons Guiding Sheath for a Left Carotid Approach in Patients With an Aberrant Right Subclavian Artery: A Technical Note on a Case of Preoperative Embolization of Intracranial Meningioma. Sase T, Ito H, Wakatsuki K, Nakamura H, Murata H.Cureus. 2025 Jan 24;17(1):e77944. doi: 10.7759/cureus.77944. eCollection 2025 Jan.PMID: 39996182
-
Left Distal Transradial Approach for the Treatment of a Sacral Extradural Arteriovenous Fistula: A Technical Note and Literature Review.Ito H, Uchida M, Kaji T, Fukano T, Hagiwara Y, Takasuna H, Murata H.World Neurosurg. 2023 Jun;174:25-29. doi: 10.1016/j.wneu.2023.02.141. Epub 2023 Mar 7.PMID: 36894006
-
Initial Experience with Left Transradial Neurointerventions for Cerebral Aneurysms Using the 6-French Simmons Guiding Sheath. Uchida M, Ito H, Takasuna H, Goto T, Takumi I, Fukano T, Hagiwara Y, Tanaka Y.J Stroke Cerebrovasc Dis. 2022 Apr;31(4):106350. doi: 10.1016/j.jstrokecerebrovasdis.2022.106350. Epub 2022 Feb 10.PMID: 35152132
-
Left Transradial Neurointerventions Using the 6-French Simmons Guiding Sheath: Initial Experiences with the Interchange Technique. Ito H, Uchida M, Takasuna H, Goto T, Takumi I, Fukano T, Hagiwara Y, Tanaka Y.World Neurosurg. 2021 Aug;152:e344-e351. doi: 10.1016/j.wneu.2021.05.110. Epub 2021 Jun 1.PMID: 34087460